サステナビリティ
自社の事業基盤の強化
製品の品質向上
方針・考え方
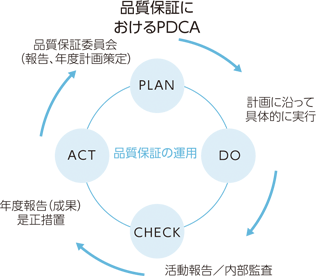
当社および関係会社は、品質方針として「お客様に満足していただける商品とサービスを提供する」ことを定めています。これをもとに中期品質目標とマテリアリティに対するKPIを設定し、品質活動に取り組んでいます。また、PDCAサイクルに沿った年間計画を実行することで、継続的にマネジメントシステムと業務の改善を進めています。
今後も、ますます多様化、高度化する市場の要求への対応力を強化し、社会に貢献する企業としてさらなる成長を図っていきます。
品質方針
「お客様に満足していただける商品とサービスを提供する」
品質目標(品質方針の実現)Q・S・G
- 継続的改善による品質活動指標の向上 - Quality -(Q)
- お客様と社会の期待に応える - Social -(S)
- 品質文化の醸成とルールの周知・遵守の徹底 - Governance -(G)
マテリアリティ:製品品質の向上への取り組みとKPI
- 重大クレームの未然防止:重大クレーム数ゼロ件
- 品質不正・データ改ざんの未然防止:
品質教育受講率 100%
理解度テスト正解率 90%以上 - 品質意識調査:不正防止意識向上 100%
体制
当社の品質保証体制はISO9001 (QMS)※を基盤としています。当社各工場においてISO9001の認証を取得し、審査機関による維持・更新を重ねています。
各工場に製造部門とは独立した品質保証部門を設置し、それぞれの品質保証部門が責任をもって各製品の品質を検査するとともに、全社の品質保証活動を統括する本社の品質保証部門が、各工場および関係会社に対して品質監査を行っています。また、全社的な品質保証活動推進のため、品質保証委員会を定期的に開催しており、当社および関係会社の活動結果、監査結果およびその改善状況やクレーム情報とその是正状況が報告され、次年度の品質保証に関する活動方針などが討議されます。討議の内容は取締役会に報告され、経営陣からのマネジメントレビューのもと、さらなる改善を図ることで、万全の体制を整えています。
- 品質マネジメントシステムの国際規格
指標
クレーム事例数
| 分類 | 2022年度 | 2023年度 | 2024年度 |
|---|---|---|---|
| 機能・成分 | 4 | 2 | 7 |
| 異物 | 3 | 4 | 2 |
| 容器・包装 | 13 | 28 | 29 |
| 納入 | 12 | 9 | 6 |
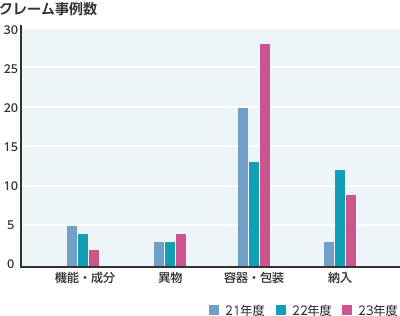
同一内容は1事例でカウント
同一内容は1事例でカウント
2022年度までクレーム事例数はやや減少傾向にありましたが、2023年度はクレーム件数が増加しました。これは、2023年度の苦情情報電子管理システム更新時に社内教育を実施した結果、社内の苦情情報への感度が高まったことによるもので、より一層適切な苦情対応ができるようになったと考えています。2024年度は、包装、納入などのクレームが、依然として高い比率を占めています。
重大なクレームは、2022年度1件、2023年度ゼロ、2024年度3件でした。今後も重大クレームゼロをKPIに掲げ、未然防止に取り組んでいきます。
取り組み
当社は、Q・S・Gのキーワードを掲げ、品質方針である「お客様に満足していただける商品とサービス提供」の実現に向けた取り組みを推進しています。
品質不正・データ改ざん防止(G)
2020年度に有償出荷品の品質管理に関わる不正・改ざん防止を目的としたガイドラインを策定し、運用を開始しています。2021年度は、社内監査で運用状況の確認を行いました。また、近年、検査データ偽装などが大きな社会問題となっていることから、2021年度に検査結果、検査データ、規格の根拠の整合を、2022年度~2024年度にかけて、承認書等の当局届出内容または顧客要求事項と製造記録の整合を確認し、品質管理に関わる不正・不適切な行為の有無を確認しました。不正や不整合は認められず、軽度の不備、潜在リスクについては改善指導を行いました。
また、各工場においては、人の手を介するマニュアル操作/作業を削減する、試験室情報管理システム(LIMS)等の導入により検査データ取り扱いの完全性を高めるなど、誤り・不正・改ざんが起こりにくい仕組みの整備を進めています。LIMS等を使用していない部箇所においても、電子署名システムを用いた試験成績書の発行管理体制を構築して確認・承認ログを取得することで、検査データ改ざんの防止を図っています。
品質文化の醸成(S,G)
社員一人一人の品質を意識した行動の促進を目的として、2021年に品質行動規範を制定しトップメッセージとして発信しました。また、2022年度は全社的に「品質不正」教育や、事業部や製造拠点に対して、変更に起因する品質リスクを低減させることを目的とした、「変更管理」に関する教育を実施しました。2023年度には、全社的に「品質行動規範」についての教育を行うとともに、研究所を対象とした「変更管理」に関する教育を、2024年度は、製品の品質に係わる、研究、企画、開発、調達、生産、物流、営業部門を対象として、世の中で起きている「品質不正の事例」教育を実施しました。今後も品質コンプライアンスについて、全社的に社内教育を展開していきます。
物流及び供給者管理(Q,S)
製造した製品自体の品質だけでなく、包材、輸送、添付文書、顧客での機能発揮も製品の一部と捉え、トータルの品質保証を目指しています。
当社の品質異常は、荷造り工程から輸送作業に起因する比率が高いですが、作業方法の見直しや作業者教育だけではヒューマンエラーがなかなか減りません。異常事例の解析を行い、委託物流業者と改善ターゲットを共有し、改善を図っていきます。
また、工場と共に当社製品製造を担う委託製造先を含めた供給者の管理については、社内ガイドラインに基づき、品質監査等を実施し、管理しています。
規制当局に対する対応(S,G)
当社は医薬品関連の各種業許可を取得しており、米国食品医薬品局(FDA)査察、医薬品医療機器総合機構(PMDA)査察、都道府県庁査察を受審し、当社の医薬品に関わる品質保証体制が規制要求を満たす水準にあることが確認されています。
研究所の品質データ保証(Q,S,G)
生物科学研究所は農薬の登録申請資料に記載する試験成績を作成可能な試験施設として、農林水産省による適合確認を受けています。また、物質科学研究所および生物科学研究所では厚生労働省が定める基準に従い医薬品申請資料の作成を行います。独立性の高い本社の品質保証部門がこれらのデータ確認を行うことにより、信頼性の高い申請資料を作成し、規制当局に提出しています。
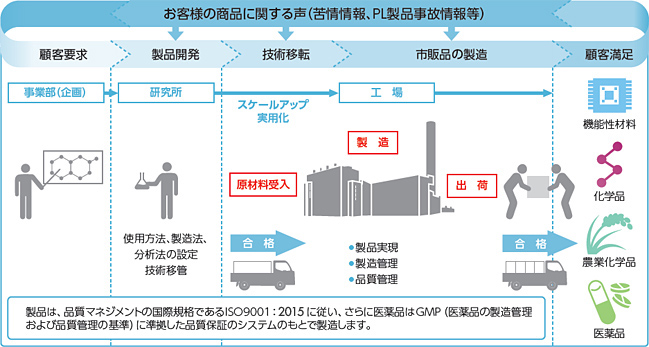
社内の品質情報ネットワーク(Q,S)
当社はお客様の商品に関する声 (苦情情報) を迅速に収集、評価し、必要な是正を実施するための社内ネットワークを構築しています。お客様からのご意見は、このネットワークにより迅速に営業、製造、品質管理の各部門に伝達され、お客様への対応、品質の改善に活用しています。
また、お客様の苦情に加え、社内の品質トラブル全般及び是正・予防措置、供給者管理情報、品質関連文書を一元管理する全社品質関連システムを2023年度より導入し、従来のシステムから新システムに移行しました。今後もより安全で高品質な製品をお客様へご提供するため、さらなる継続的改善を進めていきます。